Test antigénique Fecal Dx.
Pour une détection précoce et précise des parasites intestinaux les plus pertinents sur le plan clinique, même avant qu’il y ait présence d’œufs1–3.


Dépistez avec précision la plupart des parasites intestinaux les plus communs et pertinents sur le plan clinique.
Les tests antigéniques Fecal Dx détectent les antigènes spécifiques des parasites plutôt que de se limiter à la présence et à la détection des œufs. Un plus grand nombre d’infections peuvent être détectées plus tôt, même chez les animaux de compagnie qui semblent en parfaite santé1-3.
Le Companion Animal Parasite Council (CAPC) est d’avis que les tests antigéniques constituent une approche diagnostique de pointe. Il ne recommande pas la flottation passive, qui peut ne pas détecter toutes les infections parasitaires et qui est donc susceptible de mener à des erreurs de diagnostic4.

Les parasites
n’ont pas d’avenir.
C’est la vérité. Les tests antigéniques fécaux représentent l’avenir du dépistage des parasites tel qu’on le connaît, car ils permettent de détecter deux fois plus d’infections. Et après une étude rétrospective de près de 900 000 cas dans le cadre de laquelle les tests antigéniques fécaux ont été comparés à la flottation, nous avons maintenant les données pour le prouver5.
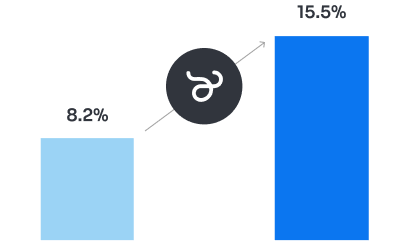
Détectez jusqu’à deux fois plus d’infections à un stade plus précoce qu’avec la flottation fécale5†.
Une étude que vous voudrez étudier.
Consultez ici nos plus récentes découvertes sur la supériorité des tests antigéniques par rapport à la flottation :

Diagnostic des infections
parasitaires intestinales.
Pour en savoir plus sur les cycles de vie des parasites, la façon dont ceux-ci se présentent, les recommandations du CAPC, la façon de réduire le risque d’infections et beaucoup plus encore, téléchargez notre guide de référence clinique.
Télécharger†Positivité antigénique cumulative pour 6 antigènes/tout résultat positif en matière d’œufs et de parasites (OP) = 1,9 x plus.
Positivité antigénique cumulative pour 6 antigènes/tout résultat positif OP relatif aux mêmes parasites : 2,3 x plus.
Références
- Elsemore D, Bezold T, Geng J, Hanna R, Tyrrell P, Beall M. Immunoassay for detection of Dipylidium caninum coproantigen in dogs and cats. J Vet Diagn Invest. 2023;35(6):671–678. doi:10.1177/10406387231189193
- Elsemore DA, Geng J, Flynn L, Cruthers L, Lucio-Forster A, Bowman DD. Enzyme-linked immunosorbent assay for coproantigen detection of Trichuris vulpis in dogs. J Vet Diagn Invest. 2014;26(3):404–411. doi:10.1177/1040638714528500
- Elsemore DA, Geng J, Cote J, Hanna R, Lucio-Forster A, Bowman DD. Enzyme-linked immunosorbent assays for coproantigen detection of Ancylostoma caninum and Toxocara canis in dogs and Toxocara cati in cats. J Vet Diagn Invest. 2017;29(5):645–653. doi:10.1177/1040638717706098
- Companion Animal Parasite Council. General guidelines for dogs and cats. 16 septembre 2022. Consulté le 24 mars 2025. www.capcvet.org/guidelines/general-guidelines
- Burton KW, Michael H, Drake C. The utility of coproantigen testing in screening populations. Vet Parasitol. Publié en ligne le 4 avril 2025. doi:10.1016/j.vetpar.2025.110459